UDDO – Central de Atendimento
11 3254 6800
Caros Pacientes,
Nosso sistema foi atualizado para continuar atendendo com excelência e a qualidade que você merece.
Para ver o resultado do seu exame basta clicar no botão ao lado ou acessar o link: resultados.uddo.com.br e digitar o login e a senha que consta em seu comprovante de retirada.
Caso tenha realizado seu exame anterior à 31/12/2021 por favor, entre em contato com os canais ao lado com nome completo, CPF e data de nascimento do paciente.
Nosso time terá prazer em atendê-lo.
Consultas & Exames
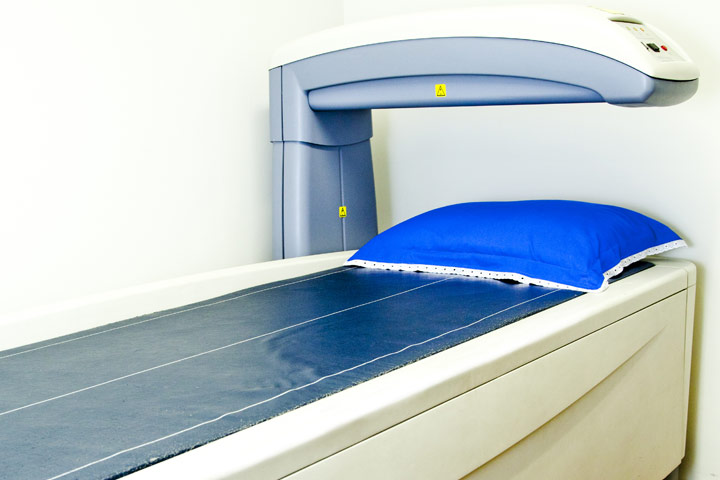
- Densitometria óssea (um segmento).
- Densitometria óssea – corpo inteiro (avaliação de massa óssea ou de composição corporal).
- Densitometria óssea – rotina: coluna e fêmur (dois segmentos).
CARDIOLOGIA
- Cintilografia de perfusão miocárdica com MIbi e Tálio – estresse e repouso
- Cintilografia cardíaca com Pirofosfato
- Cintilografia sincronizada das câmaras cardíacas – repouso
- Cintilografia cardíaca com Gálio-67
- Ventriculografia radioisotópica
- Angiografia radioisotópica
- Cintilografia do miocárdio – necrose (infarto agudo)
GASTROENTEROLOGIA
- Cintilografia para pesquisa de refluxo gastroesofágico (com ou sem aspiração pulmonar)
- Cintilografia das glândulas salivares
- Cintilografia do fígado e baço
- Cintilografia do fígado e vias biliares
- Cintilografia para detecção de hemorragia digestiva
- Cintilografia para determinação do tempo de esvaziamento gástrico (líquido ou sólido)
- Cintilografia para estudo de trânsito esofágico
- Cintilografia para pesquisa de divertículo de Meckel
ONCOLOGIA/INFECTOLOGIA
- Cintilografia do corpo inteiro com análogo de somatostatina (Octreoscan)
- Cintilografia com Gálio-67 (corpo inteiro, pulmonar ou cardíaca)
- Cintilografia com MIBG com Iodo-131 ou Iodo-123
ENDOCRINOLOGIA
- Cintilografia da tireóide e captação com Iodo131 ou Tecnécio99m
- Cintilografia das paratireóides
- Cintilografia para pesquisa de corpo inteiro (PCI) com Iodo131 ou Iodo123
MÚSCULO – ESQUELÉTICO
- Cintilografia óssea
- Cintilografia óssea Trifásica
- Cintilografia óssea com Spect
NEUROLOGIA
- Cintilografia de perfusão cerebral (SPECT cerebral)
- Cintilografia de perfusão cerebral para avaliação de doença de Parkinson (TRODAT)
- Cisternocintilografia
UROLOGIA
- Cintilografia renal dinâmica (DTPA)
- Cintilografia renal estática (DMSA)
- Cintilografia testicular
- Cistocintilografia direta
- Cistocintilografia indireta
PET
- Oncológico
- Cardiológico
- Neurológico
- Para avaliação de processos inflamatórios/infecciosos
PULMONAR
- Cintilografia pulmonar (perfusão)
- Cintilografia pulmonar (inalação)
- Cintilografia para pesquisa de shunt pulmonar
TERAPIAS
- Tratamento complementar do câncer da tireoide com Iodo131 (Iodoterapia)
- Tratamento do hipertiroidismo por doença de Graves ou Plummer com Iodo131
- Tratamento de tumores neuroendócrinos com Octreotato- Lutécio177
- Tratamento paliativo da dor óssea por metástases de câncer de mama, próstata, etc com Samário-153
- Tratamento de neuroblastoma com MIBG- Iodo131
- Tratamento de pacientes com metástases ósseas de câncer de próstata resistente à castração com XOFIGO- Rádio223
- Tratamento de pacientes com metástase óssea, linfonodal ou visceral de câncer de próstata resistente à castração com PSMA- Lutécio177
OUTROS
- Dacriocintilografia
- Linfocintilografia de membros superiores e inferiores
- Mamografia associada a Punção e Marcação Pré-cirurgica Orientada por Estereotaxia, US
- Core Biospy
- Mamotomia por esteriotaxia ou por ultrassom
- Biopsia percutânea de fragmento mamário por agulha grossa (core biopy) orientada por esterotaxia ou por Ultrassom
- Marcação pré cirurgica por nódulo esteriotaxia
- Punção ou biópsia mamária percutânea por agulha orientada por esteriotaxia ou por Ultrassom
- Punção biópsia /aspirativa de órgão ou estrutura orientada por US
- Abdome inferior feminino
- Abdome inferior masculino
- Abdome superior
- Abdome total
- Aparelho urinário
- Articulações
- Doppler Colorido de órgão ou estruturas isoladas
- Doppler Colorido de vasos cervicais arteriais bilateral
(carótida e vértebra)
- Obstétrica
- Doppler Colorido de vasos cervicais venoso bilateral
(subclávis e jugulares) - Estruturas superficiais(cervical ou axilas ou músculo)
- Glândulas salivares(todas)
- Mamas
- Órgãos superficiais (tireoide ou escroto ou penis ou crânio)
- Próstata (via abdominal)
- Transvaginal (útero, ovário , anexos e vagina)
- Transvaginal para controle de ovulação ( 3 ou mais exames)
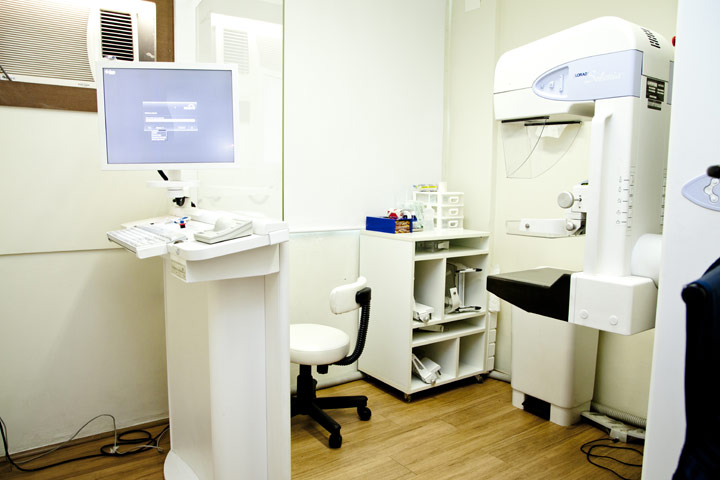
- Mamografia digital bilateral
- Mamografia digital bilateral
Convênios
- ADVANCE
- AFRESP
- ALLIANZ
- AMIL
- APEOESP
- ASSOC. DOS FUNC. PÚBLICOS
- AMPLA
- BRADESCO SAÚDE
- BLUE MED SAÚDE
- CABESP
- CARE PLUS
- CAASP
- CASSI
- CETESB
- CNEN/IPEN
- CLÍNICA DA CIDADE
- CRUZ AZUL
- COMIGO SAÚDE
- CIA DA CONSULTA
- DONA SAÚDE
- ECONOMUS
- GARANTIA SAÚDE
- GEAP
- GOLDEN CROSS
- HOSPITAL SÃO CRISTOVÃO
- MEDTOUR SAÚDE
- MEDSÊNIOR
- MEDICAL HEALTH
- MEDISERVICE
- METRUS
- NIPOMED
- NOTRE DAME-INTERMÉDICA
- OMINT
- OPEN LINE
- PLENA SAÚDE
- PORTO SAÚDE
- PREVENT SÊNIOR
- SÃO MIGUEL SAÚDE
- SAÚDE CAIXA
- SBC SAÚDE
- SEPACO AUTOGESTÃO
- SEPACO SAÚDE
- SUL AMÉRICA
- SEGUROS UNIMED
- SPA SAÚDE
- TOTAL MEDCARE
- TRASMONTANO
- UNAFISCO SAÚDE
- VIVEST
- VALE SAÚDE
CORPO CLÍNICO
Médicos Radiologistas
DR. JOSE RICARDO ANIJAR – CRM 65.477
- Formado pela Faculdade de Medicina da Universidade Federal do Pará.
- Residência Médica em Radiologia pelo Hospital Servidor Público Estadual
DRA. SILVANA HABIB GEORGES – CRM 73.359
- Formada pela Faculdade de Medicina de Santos
- Residência Médica em Radiologia pelo Hospital Heliópolis de São Paulo
DRA. SILVIA GOMES MAZZAROLO – CRM 75.809
- Formada pela Faculdade de Medicina da Santa Casa de Misericórdia de São Paulo
- Residência Médica em Radiologia pela Santa Casa de Misericórdia de São Paulo
Médicos Nucleares
DRA. MARÍLIA M. S. MARONE – CRM 18.859
- Formada pela Faculdade de Medicina da Santa Casa de Misericórdia de São Paulo
- Residência Médica em Medicina Nuclear pelo Hospital das Clínicas da FMUSP
SHLOMO LEWIN – CRM18.878
- Formado pela Faculdade de Medicina da Santa Casa de Misericórdia de São Paulo
- Residência Médica em Medicina Nuclear pelo Hospital das Clínicas da FMUSP
JOSÉ SOARES JUNIOR – CRM 44.715
- Formado pela Faculdade de Medicina da Universidade Estadual de Londrina
- Residência Médica em Medicina Nuclear pelo Hospital das Clínicas da FMUSP
DRA. IRENE SHIMURA ENDO – CRM 72.613
- Formada pela Faculdade de Medicina da Pontifícia Universidade Católica de Campinas
- Residência Médica em Medicina Nuclear pelo Hospital das Clínicas da FMUSP
DRA. MÁRCIA G. MODESTO – CRM 75.412
- Formada pela Faculdade de Medicina da Universidade Federal da Bahia
- Residência Médica em Medicina Nuclear pelo Hospital das Clínicas da FMUSP
DRA. VERENA PINTO BRITO RIBEIRO – CRM 114.277
- Formada pela Faculdade de Medicina da Universidade Federal do Pará
- Residência Médica em Medicina Nuclear pelo Hospital das Clínicas da FMUSP
DRA. FABIANA LUCAS BUENO – CRM 142.189
- Formada pela Faculdade de Medicina da Universidade Católica de Pelotas
- Residência Médica em Medicina Nuclear pelo Hospital das Clínicas da FMUSP
Médicos Cardiologistas
DR. LUCIANO HARARY – CRM 49.882
- Formado pela Faculdade de Medicina da Universidade Federal de São Paulo
- Residência Médica em Cardiologia pelo Hospital do Servidor Público Estadual
História
A UDDO foi fundada em 30 de setembro de 1988 pelos doutores Marilia M.S. Marone e Shlomo Lewin e desde sempre primou pela excelência técnica e atendimento personalizado a seus pacientes.
Inicialmente estabelecida na rua Itapeva como uma clinica de Densitometria Óssea, com o passar do tempo evoluiu para uma sociedade de médicos e passou a oferecer novos serviços:
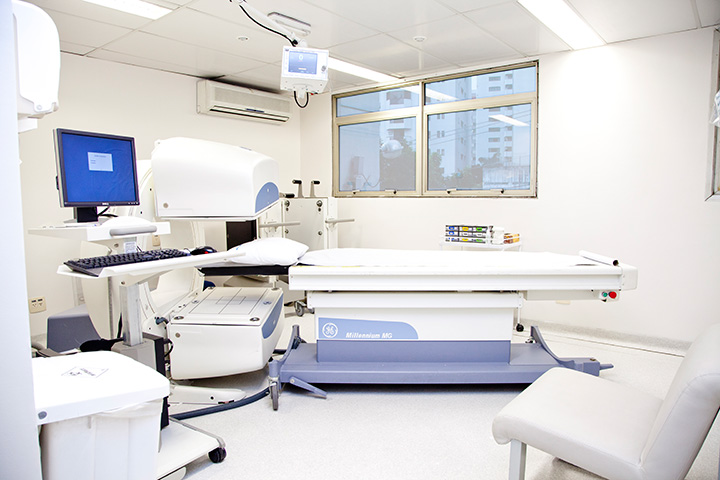
- Exames (Cintilografias) e Terapias em Medicina Nuclear,
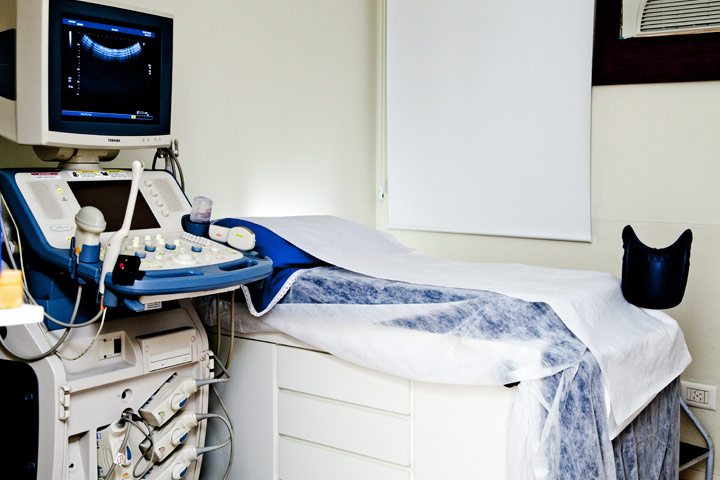
- Ultrassonografias
- Mamografias, Mamotomias, Estereotaxias e
- Biópsias
Atualmente a UDDO, além da unidade na rua Itapeva, conta com mais três unidades localizadas dentro dos Hospitais Samaritano Higienópolis (no bairro de mesmo nome), IBCC (no bairro da Moóca) e Santa Virginia (no bairro do Belém).
A UDDO tem como missão o aprimoramento de suas técnicas, buscando sempre a excelência na qualidade de seus serviços para atender melhor seus pacientes.
Fotos
Unidades
UDDO – UNIDADE ITAPEVA
Rua Itapeva, 366 – Térreo e 2º andar-conj. 24
Medicina Nuclear/Densitometria Óssea/ Radiologia
Bela Vista, São Paulo
CEP: 01232-010
2º à 6º das 7:30 hs às 18:00 hs
UDDO – UNIDADE HOSPITAL SAMARITANO
Rua Conselheiro Brotero, 1.486 – Andar P2
Medicina Nuclear/Densitometria Óssea
Higienópolis, São Paulo
CEP: 01232-010
2º à 6º das 8:00 hs às 18:00 hs
UDDO – UNIDADE INSTITUTO BRASILEIRO DE CONTROLE DO CÂNCER (IBCC)
Avenida Alcântara Machado, 2576
Medicina Nuclear/ PET-CT
Moóca, São Paulo
CEP: 03120-002
2ª à 6ª das 08:00 hs as 20:00 hs
CONTATO
Para envio de mensagem escolha Fale Conosco no campo abaixo.
Para envio de currículo selecione Trabalhe Conosco.
- Se quiser saber mais sobre nossa política de privacidade, clique aqui.